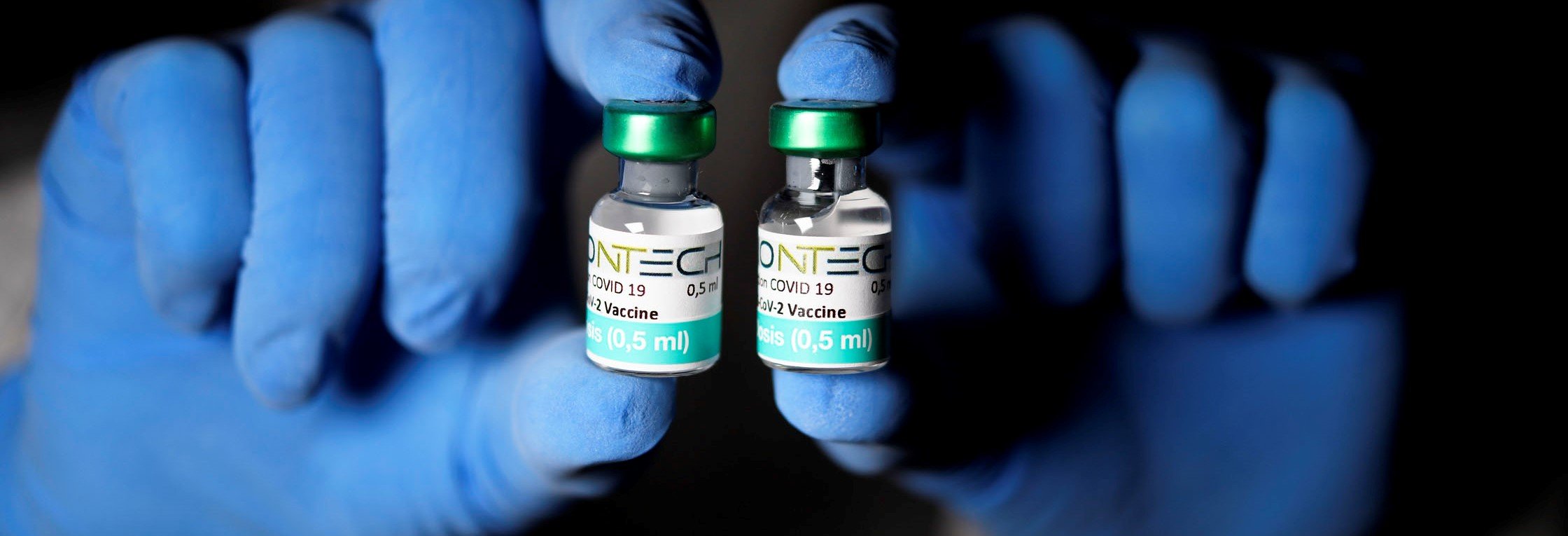
London – Pfizer und Biontech haben nach eigenen Angaben mit London eine Lieferung von 40 Millionen Impfstoffdosen vereinbart. Die Dosen sollen schrittweise geliefert werden. Die beiden Unternehmen kündigten an, sofort mit der Auslieferung ihres Impfstoffs zu beginnen. Die ersten Lieferungen sollen in wenigen Tagen im Vereinigten Königreich eintreffen.
Großbritannien wird von einer Pfizer-Produktionsstätte in Belgien aus beliefert werden. Der mRNA-Impfstoff BNT162b2 muss bei minus 70 Grad Celsius gelagert und transportiert werden. Für den Versand wurden spezielle temperaturstabile Versandeinheiten entwickelt, die die empfohlenen Temperaturbedingungen ohne zusätzliches Equipment bis auf Trockeneis aufrechterhalten können.
Die Behälter können ungeöffnet die empfohlene Temperatur für zehn Tage aufrechterhalten, was einen weltweiten Transport ermöglicht. Einmal geöffnet können die Impfzentren die Versandeinheit für die temporäre Aufbewahrung verwenden und die empfohlenen Lagerbedingungen (-70°C±10°C) für bis zu 30 Tage aufrechterhalten, indem sie den Behälter gemäß der Gebrauchsanweisung alle fünf Tage mit Eis auffüllen.
Jede Versandeinheit beinhaltet einen GPS-fähigen Temperatursensor, um den Standort und die Temperatur einer jeden Impfstofflieferung auf ihrer vorher festgelegten Route rund um die Uhr zu überwachen. Aufgetaut kann der Impfstoff bis zu fünf Tage bei zwei bis acht Grad Celsius im Kühlschrank gelagert werden.
Großbritannien ist damit das erste westeuropäische Land, welches Impfungen gegen Großbritannien hat heute die temporäre Notfallzulassung für den Coronaimpfstoff des Mainzer Pharmaunternehmens Biontech und seines US-Partners Pfizer erteilt. Es ist die weltweit erste Notfallzulassung eines in einer Phase-III-Studie getesteten SARS-CoV-2-Vakzins. erlaubt. Chief Business Officer und Chief Commercial Officer Sean Marett betonte bei einer Online-Pressekonferenz aber, dass nun nicht alle Impfstoffbestände an Großbritannien gehen würden. „Jedes Land wird einen fairen Anteil erhalten“.
„Die Notfallzulassung im Vereinigten Königreich ermöglicht es zum ersten Mal, dass Bürgerinnen und Bürger außerhalb von klinischen Studien die Möglichkeit haben, sich gegen COVID-19 immunisieren zu lassen“, sagte Ugur Sahin, CEO und Mitbegründer von Biontech.
Die Entscheidung der britischen Zulassungsbehörde MHRA basiert auf einem rollierenden Review, der auch Daten aus einer Phase-III-Studie umfasst. Sie zeigt bei Probanden ohne vorherige SARS-CoV-2-Infektion einen Impfschutz von 95 Prozent.
Wirksamkeit in allen Altersgruppen gezeigt
Die Wirksamkeit der Impfung sei über alle Alters- und Geschlechtsgruppen in der gesamten diversen Studienpopulation konsistent gewesen, so die Angaben von Biontech und Pfizer. BNT162b2 sei in der Studie generell gut vertragen worden. Bislang konnte das Data Monitoring Committee keine schwerwiegenden Nebenwirkungen feststellen.
Nach Angaben der beiden Unternehmen können noch in diesem Jahr weltweit bis zu 50 Millionen Impfstoffdosen ausgeliefert werden, sowie bis zu 1,3 Milliarden Dosen bis Ende 2021.
Biontech und Pfizer haben ebenso wie das US-Unternehmen Moderna auch in den USA und der EU Anträge auf eine Notfallzulassung beziehungsweise bedingte Zulassung ihrer Impfstoffe gestellt. Sie rechnen noch im Dezember mit Entscheidungen der beiden zuständigen Behörden in den USA und der EU.
Ärzteblatt
Foto: picture alliance, Laci Perenyi